人骨肉瘤
发布时间:2023-03-21 09:59:47 人气:2029
Adv. Sci. 2023:COF基材料用于肿瘤铁死亡和铁增强声动力疗法

背景
共价有机框架(COFs)在生物医学领域的应用越来越受到人们的关注。以COFs为基础的纳米增敏剂具有均匀的纳米级形态和肿瘤特异性疗效,然而,它们的合成仍然具有挑战性。在本研究中,以可控的方式合成了不同的COF纳米碗,并设计成具有肿瘤特异性声动力学活性的可激活纳米增敏剂。高结晶度保证了COF纳米碗的有序多孔结构,从而有效地装载了小分子声敏剂Rose Bengal (RB)。为了避免对正常组织的非特异性损伤,在负载RB的COFs上原位生长的氧化锰(MnOx)特异性地抑制了声敏化效应。与肿瘤过表达谷胱甘肽(GSH)反应后,“看门人”MnOx在超声照射下迅速分解,恢复COF纳米增敏剂的活性氧(ROS)生成能力。增加细胞内活性氧应激和谷胱甘肽消耗同时诱导铁死亡,以提高声动力功效。此外,非常规的碗状形态使纳米致敏剂增强了肿瘤的积聚和保留。肿瘤特异性声动力治疗与铁死亡相结合,在杀伤癌细胞和抑制肿瘤生长方面具有很高的疗效。
图文导读
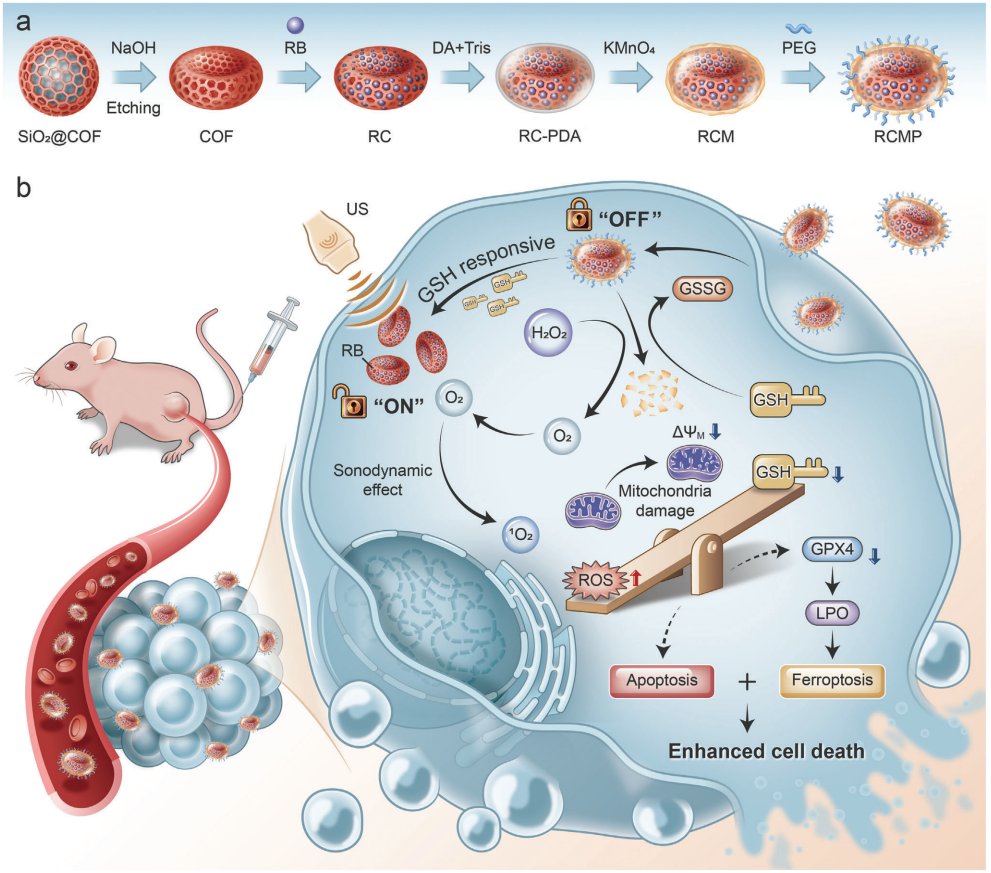
(图1 可活化纳米增敏剂RCMP的制备及治疗应用示意图)
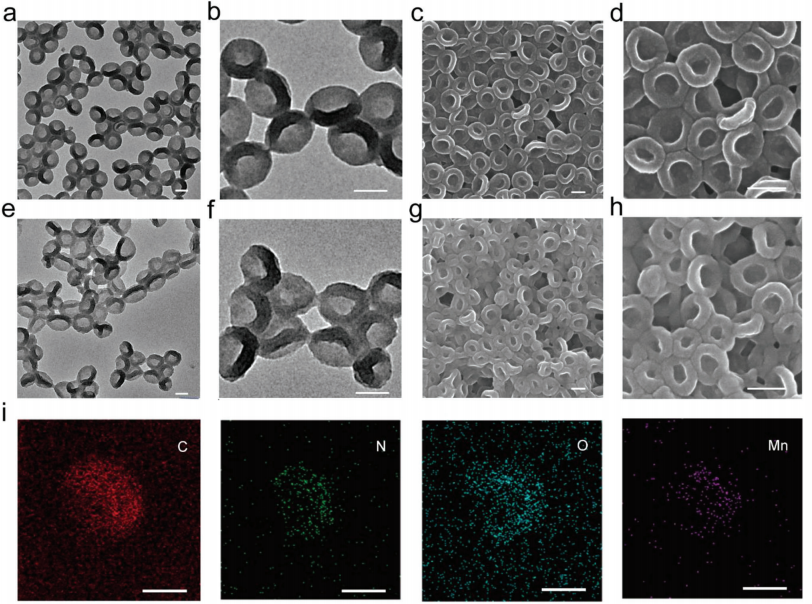
(图2 纯的和功能化的碳纳米碗的表征)
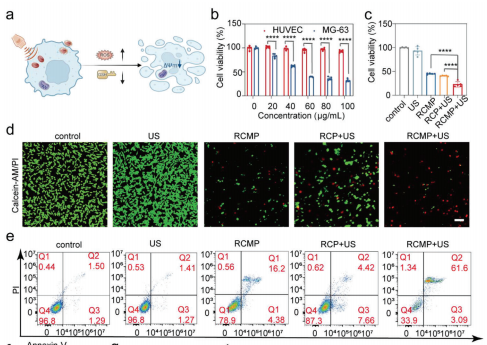
(图3 RCMP激活SDT的体外治疗效果增强。)
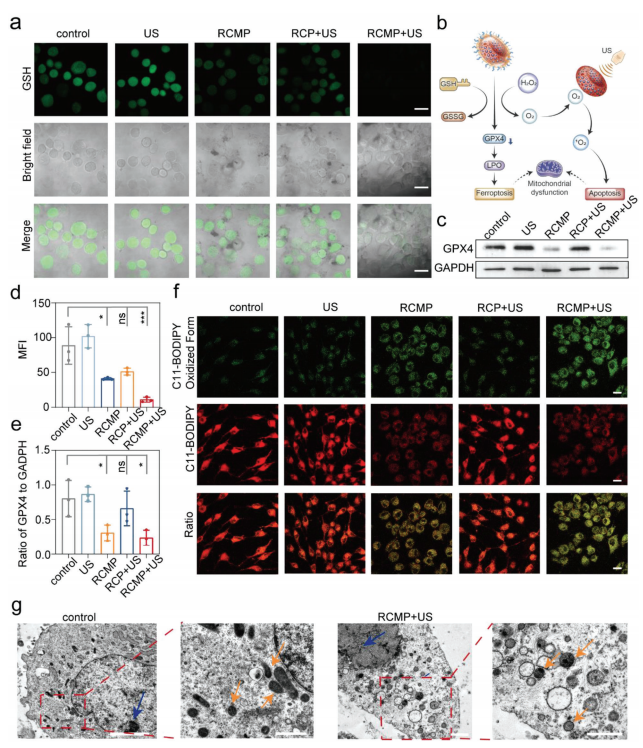
(图4 RCMP介导SDT的铁死亡机制)
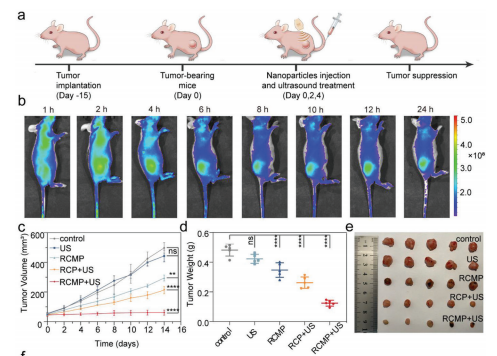
(图5 RCMP介导的铁凋亡增强SDT的体内抗肿瘤效果)
全文总结
成功地合成了一种基于COF纳米碗的纳米敏化剂,它具有独特的纳米级形态和可激活的声动力活性。COF纳米碗具有高结晶度和丰富的孔隙度,可以有效地装载小分子声敏剂RB。通过对负载RB的COF纳米碗进行MnOx壳层改造,获得了可活化的纳米敏化剂。得益于GSH响应降解行为,MnOx可以作为可拆卸的“看门人”来阻断RCMP的声动力效应。肿瘤特异性纳米增敏剂在US照射下从“关”状态切换到“开”状态,在肿瘤部位发挥治疗效果,使gsh激活的声动力过程得以实现,同时诱导GPX4下调。体外实验显示RCMP联合US照射可破坏细胞内氧化还原止血,引起癌细胞铁死亡。这些协同作用增强了治疗效果。体内评估也证实了碗状的形态使得COF纳米增敏剂对肿瘤的积累和保留有特殊的增强作用。因此,RCMP在US照射下表现出抑制肿瘤生长的高效能。总的来说,本研究为非常规形态的COFs基纳米增敏剂的可控合成和开发铺平了道路,为实现可活化和增强铁致敏剂的SDT提供了新的策略,并扩展了纳米COFs的生物医学应用。
原文链接:https://doi.org/10.1002/advs.202206009
仅用于学术分享,侵权请联系删除,欢迎交流。
| 温馨提示:苏州北科纳米供应产品仅用于科研,不能用于人体,不同批次产品规格性能有差异。网站部分文献案例图片源自互联网,图片仅供参考,请以实物为主,如有侵权请联系我们立即删除。 |
上一篇: 乳腺癌


